दैनिक जीवन में अमीन (Amines) की महत्वपूर्ण भूमिका
क्या आपने कभी सोचा है कि आपकी दवाइयों में, सफाई के डिटर्जेंट में, या यहां तक कि आपके शरीर के प्रोटीन में कौन से रसायन छुपे हुए हैं? आज हम रसायन विज्ञान की एक ऐसी शाखा का अध्ययन करेंगे जो न केवल आपकी परीक्षा में महत्वपूर्ण है, बल्कि आपके दैनिक जीवन में भी अत्यंत उपयोगी है – अमीन (Amines)।
अमीन वे कार्बनिक यौगिक हैं जो अमोनिया (NH₃) के हाइड्रोजन परमाणुओं को कार्बन परमाणुओं से जुड़े समूहों द्वारा प्रतिस्थापित करने से बनते हैं। आपको यह जानकर आश्चर्य होगा कि डॉक्टर द्वारा दी जाने वाली एंटीबायोटिक दवाएं, आपके शरीर में DNA का निर्माण करने वाले न्यूक्लिक एसिड, और यहां तक कि वह कैफीन भी जो आपकी चाय-कॉफी में होती है – सभी में अमीन समूह मौजूद होते हैं।
इस अध्याय में हम न केवल अमीन की रासायनिक संरचना और गुणों को समझेंगे, बल्कि यह भी देखेंगे कि कैसे ये यौगिक आधुनिक चिकित्सा विज्ञान, कृषि, और औद्योगिक क्षेत्र में क्रांति ला रहे हैं। तो आइए, इस रोमांचक यात्रा की शुरुआत करते हैं!
अध्ययन के उद्देश्य (Learning Objectives)
इस अध्याय को पूरा करने के बाद आप निम्नलिखित में सक्षम होंगे:
- संरचनात्मक समझ: अमीन की संरचना, वर्गीकरण और नामकरण की पद्धति को समझना और प्राथमिक, द्वितीयक, तृतीयक अमीन के बीच अंतर करना
- भौतिक गुणधर्म: अमीन के क्वथनांक, घुलनशीलता, और हाइड्रोजन बंधन जैसे भौतिक गुणों को समझना और इनके कारणों की व्याख्या करना
- रासायनिक अभिक्रियाएं: अमीन की विभिन्न रासायनिक अभिक्रियाओं जैसे एसिड-बेस अभिक्रिया, एल्काइलेशन, एसाइलेशन और डायजोटाइजेशन को समझना
- निर्माण विधियां: अमीन के निर्माण की विभिन्न प्रयोगशाला और औद्योगिक विधियों में महारत हासिल करना
- व्यावहारिक अनुप्रयोग: दैनिक जीवन में अमीन के उपयोग और उनके औद्योगिक महत्व को समझना
- परीक्षा तैयारी: CBSE बोर्ड परीक्षा के लिए महत्वपूर्ण प्रश्न पैटर्न और उत्तर लेखन तकनीक में दक्षता प्राप्त करना
1: अमीन का परिचय और वर्गीकरण (Introduction and Classification of Amines)
अमीन क्या हैं? (What are Amines?)
अमीन को समझने के लिए पहले अमोनिया (NH₃) को याद करते हैं। अमोनिया एक पिरामिडीय आकार का अणु है जिसमें नाइट्रोजन परमाणु पर एक अकेला इलेक्ट्रॉन युग्म (lone pair) होता है। जब अमोनिया के एक या अधिक हाइड्रोजन परमाणुओं को एल्किल या एरिल समूहों द्वारा प्रतिस्थापित कर दिया जाता है, तो अमीन बनते हैं।
सामान्य सूत्र: R-NH₂, R₂NH, R₃N (जहां R = एल्किल या एरिल समूह)
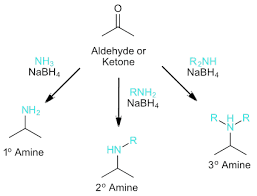
अमीन का वर्गीकरण (Classification of Amines)
अमीन को दो मुख्य आधारों पर वर्गीकृत किया जाता है:
1. प्रतिस्थापन की डिग्री के आधार पर (Based on Degree of Substitution)
प्राथमिक अमीन (Primary Amines – 1°)
- सूत्र: R-NH₂
- उदाहरण: CH₃NH₂ (मेथाइलएमीन), C₂H₅NH₂ (एथाइलएमीन)
- विशेषता: नाइट्रोजन से केवल एक कार्बन परमाणु जुड़ा होता है
द्वितीयक अमीन (Secondary Amines – 2°)
- सूत्र: R₂NH
- उदाहरण: (CH₃)₂NH (डाइमेथाइलएमीन), CH₃NHCH₂CH₃ (मेथाइलएथाइलएमीन)
- विशेषता: नाइट्रोजन से दो कार्बन परमाणु जुड़े होते हैं
तृतीयक अमीन (Tertiary Amines – 3°)
- सूत्र: R₃N
- उदाहरण: (CH₃)₃N (ट्राइमेथाइलएमीन), (C₂H₅)₃N (ट्राइएथाइलएमीन)
- विशेषता: नाइट्रोजन से तीन कार्बन परमाणु जुड़े होते हैं
2. कार्बन श्रृंखला के आधार पर (Based on Carbon Chain)
एलिफैटिक अमीन (Aliphatic Amines)
- खुली श्रृंखला वाले अमीन
- उदाहरण: CH₃NH₂, (C₂H₅)₂NH
एरोमैटिक अमीन (Aromatic Amines)
- बेंजीन रिंग से जुड़े अमीन
- उदाहरण: C₆H₅NH₂ (एनिलीन), C₆H₅N(CH₃)₂
Chemistry Check Box:
प्रश्न: (CH₃)₂NCH₂CH₃ में अमीन का प्रकार क्या है?
उत्तर: यह एक तृतीयक अमीन है क्योंकि नाइट्रोजन से तीन कार्बन परमाणु जुड़े हैं।
2: अमीन का नामकरण (Nomenclature of Amines)
IUPAC नामकरण पद्धति (IUPAC Nomenclature)
अमीन का नामकरण दो मुख्य विधियों से किया जाता है:
1. प्राथमिक अमीन के लिए (For Primary Amines)
विधि: सबसे लंबी कार्बन श्रृंखला को मूल श्रृंखला मानकर उसके नाम के अंत में ‘एमीन’ (amine) लगाया जाता है।
उदाहरण:
- CH₃NH₂ → मेथेनएमीन (Methanamine)
- CH₃CH₂NH₂ → एथेनएमीन (Ethanamine)
- CH₃CH₂CH₂NH₂ → प्रोपेन-1-एमीन (Propan-1-amine)
2. द्वितीयक और तृतीयक अमीन के लिए (For Secondary and Tertiary Amines)
विधि: छोटे समूहों को N-एल्किल के रूप में उपसर्गों के रूप में लिखा जाता है।
उदाहरण:
- (CH₃)₂NH → N-मेथाइलमेथेनएमीन (N-methylmethanamine)
- CH₃NHCH₂CH₃ → N-मेथाइलएथेनएमीन (N-methylethanamine)
- (CH₃)₃N → N,N-डाइमेथाइलमेथेनएमीन (N,N-dimethylmethanamine)
सामान्य नामकरण (Common Nomenclature)
एलिफैटिक अमीन: एल्किल समूहों के नाम के बाद ‘एमीन’ लगाया जाता है।
- CH₃NH₂ → मेथाइलएमीन (Methylamine)
- (C₂H₅)₂NH → डाइएथाइलएमीन (Diethylamine)
- (CH₃)₃N → ट्राइमेथाइलएमीन (Trimethylamine)
एरोमैटिक अमीन: विशेष नाम होते हैं।
- C₆H₅NH₂ → एनिलीन (Aniline)
- C₆H₅NHCH₃ → N-मेथाइलएनिलीन (N-methylaniline)
Common Error Alert:
छात्र अक्सर द्वितीयक और तृतीयक अमीन के नामकरण में गलती करते हैं। याद रखें कि N- उपसर्ग का मतलब है कि वह समूह सीधे नाइट्रोजन से जुड़ा है, कार्बन श्रृंखला से नहीं।
3: अमीन के भौतिक गुण (Physical Properties of Amines)
1. भौतिक अवस्था और गंध (Physical State and Odor)
निम्न अणुभार वाले अमीन:
- कमरे के तापमान पर गैसीय अवस्था में होते हैं
- तीखी, मछली जैसी गंध होती है
- जल में अत्यधिक घुलनशील होते हैं
उच्च अणुभार वाले अमीन:
- द्रव या ठोस अवस्था में होते हैं
- गंध कम तेज होती है
- जल में कम घुलनशील होते हैं
Real-World Chemistry:
मछली की तड़की गंध का कारण ट्राइमेथाइलएमीन (Trimethylamine) है। जब मछली खराब होती है, तो बैक्टीरिया प्रोटीन को तोड़कर यह अमीन बनाते हैं।
2. क्वथनांक (Boiling Point)
अमीन के क्वथनांक की तुलना:
क्रम: प्राथमिक > द्वितीयक > तृतीयक अमीन
कारण: हाइड्रोजन बंधन की मात्रा
हाइड्रोजन बंधन का प्रभाव (Effect of Hydrogen Bonding)
प्राथमिक अमीन:
- दो N-H बंध होते हैं
- अधिकतम हाइड्रोजन बंधन बनाते हैं
- सबसे ऊंचा क्वथनांक
द्वितीयक अमीन:
- एक N-H बंध होता है
- मध्यम हाइड्रोजन बंधन
- मध्यम क्वथनांक
तृतीयक अमीन:
- कोई N-H बंध नहीं
- केवल वैन डर वाल्स बल
- सबसे कम क्वथनांक
3. जल में घुलनशीलता (Solubility in Water)
घुलनशीलता का क्रम: प्राथमिक > द्वितीयक > तृतीयक अमीन
व्याख्या:
- प्राथमिक अमीन जल के साथ अधिकतम हाइड्रोजन बंधन बनाते हैं
- कार्बन परमाणुओं की संख्या बढ़ने पर घुलनशीलता कम होती है
- C₅ से अधिक कार्बन वाले अमीन जल में कम घुलते हैं
4. अम्लीयता और क्षारीयता (Acidity and Basicity)
अमीन क्षारीय प्रकृति के होते हैं क्योंकि नाइट्रोजन पर अकेला इलेक्ट्रॉन युग्म होता है।
क्षारीयता का क्रम (गैसीय अवस्था में): 3° > 2° > 1° > NH₃
क्षारीयता का क्रम (जलीय विलयन में): 2° > 1° > 3° > NH₃
Chemistry Check Box:
प्रश्न: एनिलीन अमोनिया से कम क्षारीय क्यों है?
उत्तर: एनिलीन में नाइट्रोजन का अकेला इलेक्ट्रॉन युग्म बेंजीन रिंग के साथ अनुनाद में भाग लेता है, जिससे इसकी उपलब्धता कम हो जाती है।
4: अमीन की तैयारी विधियां (Methods of Preparation of Amines)
1. अमोनिया की एल्काइलेशन (Alkylation of Ammonia)
अभिक्रिया:
NH₃ + R-X → RNH₃⁺X⁻ → RNH₂ + HX
RNH₂ + R-X → R₂NH₂⁺X⁻ → R₂NH + HX
R₂NH + R-X → R₃NH⁺X⁻ → R₃N + HXविशेषताएं:
- यह एक चरणबद्ध अभिक्रिया है
- मिश्रित उत्पाद प्राप्त होते हैं
- अमोनिया की अधिकता का उपयोग करना पड़ता है
सीमाएं:
- शुद्ध उत्पाद प्राप्त करना कठिन
- उत्पादों को अलग करना मुश्किल
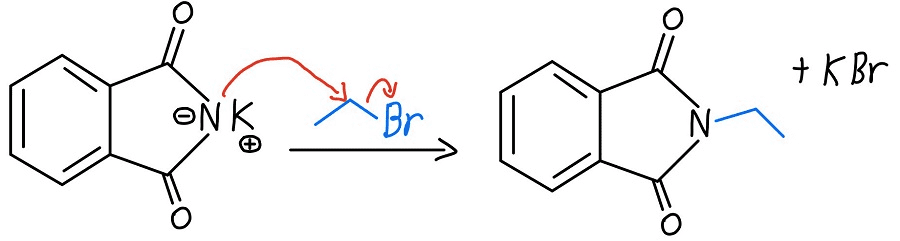
2. गैब्रिएल संश्लेषण (Gabriel Synthesis)
सिद्धांत: फ्थैलिमाइड का उपयोग करके केवल प्राथमिक अमीन बनाए जाते हैं।
Process Analysis:
- चरण 1: फ्थैलिमाइड + KOH → पोटेशियम फ्थैलिमाइड
- चरण 2: पोटेशियम फ्थैलिमाइड + R-X → N-एल्किल फ्थैलिमाइड
- चरण 3: N-एल्किल फ्थैलिमाइड + NaOH/H₂O → प्राथमिक अमीन + सोडियम फ्थैलेट
लाभ: केवल प्राथमिक अमीन बनते हैं, मिश्रित उत्पाद नहीं
3. नाइट्राइल का अपचयन (Reduction of Nitriles)
अभिक्रिया: R-CN + 4[H] → R-CH₂NH₂
अपचायक कारक:
- LiAlH₄ (शुष्क ईथर में)
- Na/C₂H₅OH (सोडियम + इथेनॉल)
विशेषता: यह विधि प्राथमिक अमीन बनाने के लिए उत्तम है
4. नाइट्रो यौगिकों का अपचयन (Reduction of Nitro Compounds)
एरोमैटिक नाइट्रो यौगिक:
C₆H₅-NO₂ + 6[H] → C₆H₅-NH₂ + 2H₂Oअपचायक कारक:
- Fe/HCl (अम्लीय माध्यम)
- Sn/HCl
- Zn/NH₄Cl
एलिफैटिक नाइट्रो यौगिक:
- LiAlH₄/ईथर का उपयोग
5. एमाइड का अपचयन (Reduction of Amides)
अभिक्रिया:
RCONH₂ + 4[H] → RCH₂NH₂ + H₂O (प्राथमिक अमीन)
RCONHR' + 4[H] → RCH₂NHR' + H₂O (द्वितीयक अमीन)अपचायक: LiAlH₄
Real-World Chemistry:
फार्मास्युटिकल उद्योग में अधिकांश दवाओं में अमीन समूह होते हैं। एस्पिरिन, पैरासिटामोल, और एंटीबायोटिक्स का निर्माण इन्हीं विधियों से होता है।
5: अमीन की रासायनिक अभिक्रियाएं (Chemical Reactions of Amines)
1. अम्ल-क्षार अभिक्रियाएं (Acid-Base Reactions)
क्षारीय गुण:
अमीन Lewis bases हैं क्योंकि नाइट्रोजन पर अकेला इलेक्ट्रॉन युग्म होता है।
R₃N + HCl → R₃NH⁺Cl⁻ (अमीन हाइड्रोक्लोराइड)
R₃N + H₂O ⇌ R₃NH⁺ + OH⁻क्षारीयता की तुलना:
- एल्किल अमीन > अमोनिया > एरिल अमीन
2. एल्काइलेशन (Alkylation)
अभिक्रिया:
RNH₂ + R'X → RNH₂R'⁺X⁻ → RNHR' + HXविशेषताएं:
- SN2 क्रियाविधि से होती है
- प्राथमिक एल्किल हैलाइड सबसे अच्छे होते हैं
3. एसाइलेशन (Acylation)
अभिक्रिया:
RNH₂ + R'COCl → RNHCOR' + HCl (N-substituted amide)हिंसबर्ग अभिक्रिया (Hinsberg Reaction):
बेंजीन सल्फोनिल क्लोराइड के साथ:
- प्राथमिक अमीन: घुलनशील उत्पाद
- द्वितीयक अमीन: अघुलनशील उत्पाद
- तृतीयक अमीन: कोई अभिक्रिया नहीं
Common Error Alert:
छात्र अक्सर एसाइलेशन और एल्काइलेशन को भ्रमित करते हैं। याद रखें:
- एल्काइलेशन में R-X का उपयोग (मिश्रित उत्पाद)
- एसाइलेशन में RCOCl का उपयोग (एक ही उत्पाद)
4. डायजोटाइजेशन (Diazotization)
केवल प्राथमिक एरोमैटिक अमीन के साथ:
C₆H₅NH₂ + NaNO₂ + 2HCl → C₆H₅N₂⁺Cl⁻ + NaCl + 2H₂O
(बेंजीन डायजोनियम क्लोराइड)परिस्थितियां: 0-5°C तापमान पर
उपयोग: डाई और अन्य एरोमैटिक यौगिकों का संश्लेषण
5. कार्बाइलएमीन अभिक्रिया (Carbylamine Reaction)
केवल प्राथमिक अमीन के साथ:
RNH₂ + CHCl₃ + 3KOH → R-N≡C + 3KCl + 3H₂O
(कार्बाइलएमीन)विशेषता: अत्यंत तीखी, अप्रिय गंध
परीक्षा: प्राथमिक अमीन की पहचान के लिए उपयोग
6: एनिलीन – एक विशेष अध्ययन (Aniline – A Special Study)
एनिलीन की संरचना (Structure of Aniline)
आणविक सूत्र: C₆H₅NH₂
विशेष संरचनात्मक गुण:
- नाइट्रोजन का अकेला इलेक्ट्रॉन युग्म बेंजीन रिंग के साथ अनुनाद करता है
- यह अनुनाद एनिलीन के अनोखे गुणों का कारण है
एनिलीन की तैयारी (Preparation of Aniline)
1. नाइट्रोबेंजीन का अपचयन
मुख्य औद्योगिक विधि:
C₆H₅NO₂ + 6[H] → C₆H₅NH₂ + 2H₂Oअपचायक कारक:
- Fe + HCl (सबसे सामान्य)
- Sn + HCl
- Zn + NH₄Cl
2. अमोनोलिसिस
अभिक्रिया:
C₆H₅Cl + NH₃ → C₆H₅NH₂ + HClपरिस्थितियां: उच्च तापमान और दबाव, Cu₂Cl₂ उत्प्रेरक
एनिलीन के रासायनिक गुण (Chemical Properties of Aniline)
1. क्षारीयता (Basicity)
एनिलीन < अमोनिया < एल्किल अमीन
कारण:
- नाइट्रोजन का अकेला इलेक्ट्रॉन युग्म बेंजीन रिंग के साथ delocalized है
- प्रोटॉन स्वीकार करने की क्षमता कम है
2. एनिलीन की एल्काइलेशन
C₆H₅NH₂ + CH₃I → C₆H₅NHCH₃ + HI3. एनिलीन की एसाइलेशन
C₆H₅NH₂ + CH₃COCl → C₆H₅NHCOCH₃ + HCl
(एसिटेनिलाइड)4. एनिलीन की ब्रोमीनेशन
जलीय विलयन में:
C₆H₅NH₂ + 3Br₂ → 2,4,6-ट्राइब्रोमोएनिलीन + 3HBrविशेषता: श्वेत अवक्षेप बनता है
एनिलीन के उपयोग (Uses of Aniline)
Real-World Chemistry:
- डाई उद्योग: मैजेंटा, मेथिलीन ब्लू जैसे रंग
- फार्मास्युटिकल: पैरासिटामोल, सल्फा ड्रग्स
- पॉलिमर: पॉलीयूरेथेन फोम
- रबर: वल्कनाइजेशन एक्सेलेरेटर
Historical Context:
एनिलीन की खोज 1826 में ओटो अनवर्डॉर्बेन ने की थी। यह पहला synthetic dye “mauveine” बनाने में उपयोग हुआ, जिसने रासायनिक उद्योग में क्रांति ला दी।
7: अमीन की पहचान परीक्षाएं (Identification Tests for Amines)
1. हिंसबर्ग परीक्षा (Hinsberg Test)
सिद्धांत: विभिन्न प्रकार के अमीन बेंजीन सल्फोनिल क्लोराइड के साथ अलग व्यवहार करते हैं।
Process Analysis:
प्राथमिक अमीन (1°):
RNH₂ + C₆H₅SO₂Cl → C₆H₅SO₂NHR + HCl- उत्पाद NaOH में घुलता है (N-H बंध उपस्थित)
- HCl मिलाने पर अवक्षेप बनता है
द्वितीयक अमीन (2°):
R₂NH + C₆H₅SO₂Cl → C₆H₅SO₂NR₂ + HCl- उत्पाद NaOH में नहीं घुलता (कोई N-H बंध नहीं)
तृतीयक अमीन (3°):
- कोई अभिक्रिया नहीं (कोई N-H बंध नहीं)
2. कार्बाइलएमीन परीक्षा (Carbylamine Test)
केवल प्राथमिक अमीन के लिए:
RNH₂ + CHCl₃ + 3KOH → RN≡C + 3KCl + 3H₂Oपहचान: अत्यंत अप्रिय गंध (isocyanide की)
3. डायजोटाइजेशन परीक्षा (Diazotization Test)
केवल प्राथमिक एरोमैटिक अमीन के लिए:
ArNH₂ + NaNO₂ + 2HCl → ArN₂⁺Cl⁻ + NaCl + 2H₂Oयुग्मन अभिक्रिया: β-नैप्थॉल के साथ लाल-नारंगी रंग
4. नाइट्रस अम्ल परीक्षा (Nitrous Acid Test)
प्राथमिक अमीन: N₂ गैस निकलती है
द्वितीयक अमीन: पीला तेल जैसा पदार्थ (N-nitroso compound)
तृतीयक अमीन: कोई दृश्य परिवर्तन नहीं
Chemistry Check Box:
प्रश्न: अज्ञात अमीन में हिंसबर्ग परीक्षा करने पर अवक्षेप बनता है जो NaOH में नहीं घुलता। यह कौन सा अमीन है?
उत्तर: द्वितीयक अमीन (2°)
8: अमीन के औद्योगिक और जैविक महत्व (Industrial and Biological Importance of Amines)
औद्योगिक उपयोग (Industrial Applications)
1. डाई और रंजक उद्योग (Dye Industry)
मुख्य उत्पाद:
- मेथिलीन ब्लू: बैक्टीरिया स्टेनिंग
- कांगो रेड: pH इंडिकेटर
- मैजेंटा: टेक्सटाइल डाई
Current Research:
आजकल नैनो-मटेरियल्स के साथ अमीन-बेस्ड डाई का उपयोग सोलर सेल्स में हो रहा है।
2. फार्मास्युटिकल उद्योग (Pharmaceutical Industry)
महत्वपूर्ण दवाएं:
- एड्रिनालीन: हृदय रोग उपचार
- एफेड्रीन: अस्थमा उपचार
- मॉर्फीन: दर्द निवारक
- निकोटीन: तंत्रिका तंत्र प्रभावित करती है
3. पॉलिमर उद्योग (Polymer Industry)
नायलॉन: हेक्सामेथिलीन डाइअमीन से
पॉलीयूरेथेन: एरोमैटिक अमीन से
जैविक महत्व (Biological Importance)
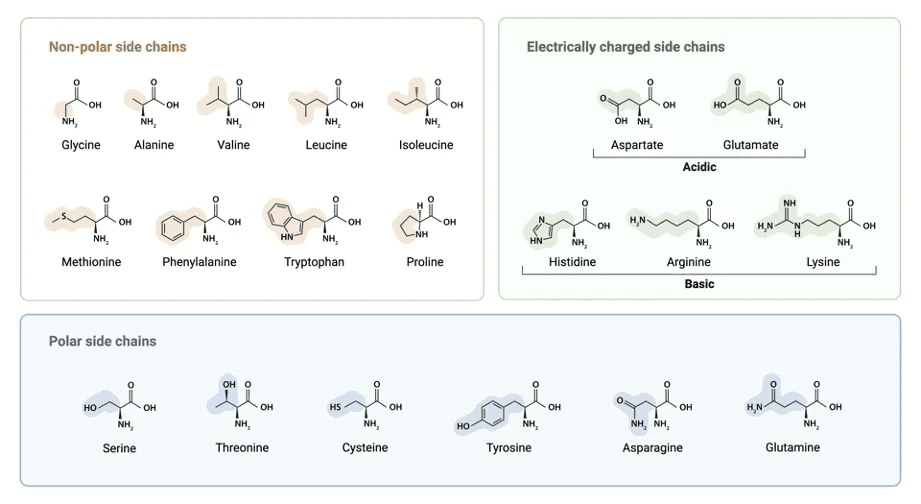
1. प्रोटीन संरचना (Protein Structure)
अमीनो एसिड: सभी प्रोटीन अमीन समूह वाले अमीनो एसिड से बने हैं
पेप्टाइड बंध: अमीन और कार्बोक्सिल समूह के बीच बनता है
2. न्यूरोट्रांसमीटर (Neurotransmitters)
डोपामीन: मूड और मोटर कंट्रोल
सेरोटोनिन: नींद और मूड नियंत्रण
नॉरएड्रिनालीन: तनाव प्रतिक्रिया
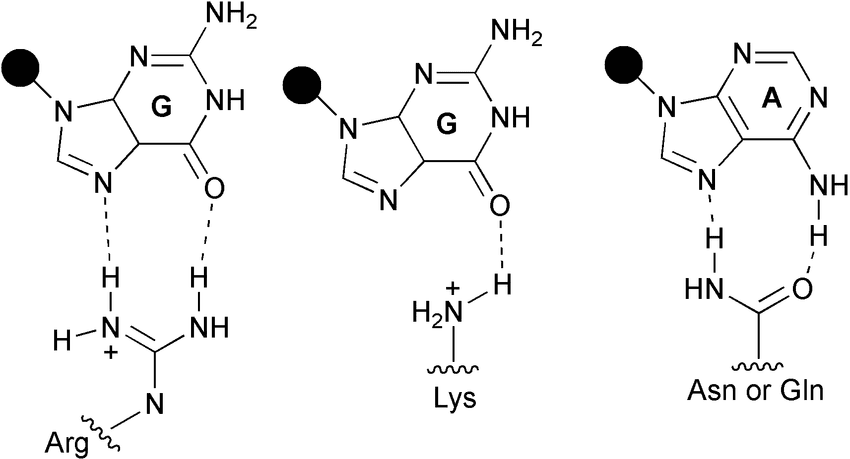
3. DNA और RNA
प्यूरीन और पिरिमिडीन: नाइट्रोजन युक्त bases में अमीन समूह
Real-World Chemistry:
मानव मस्तिष्क में डोपामीन की कमी पार्किंसन रोग का कारण बनती है। L-DOPA नामक अमीन-आधारित दवा इसका उपचार है।
पर्यावरणीय प्रभाव (Environmental Impact)
सकारात्मक प्रभाव:
- जल शुद्धीकरण में ion-exchange resins
- कृषि में बायो-डिग्रेडेबल कीटनाशक
नकारात्मक प्रभाव:
- कुछ एरोमैटिक अमीन कैंसरकारी होते हैं
- औद्योगिक अपशिष्ट में toxic amines
9: प्रैक्टिस प्रश्न और समाधान (Practice Questions and Solutions)
बहुविकल्पीय प्रश्न (Multiple Choice Questions)
प्रश्न 1: निम्नलिखित में से कौन सा यौगिक सबसे अधिक क्षारीय है?
a) NH₃
b) CH₃NH₂
c) (CH₃)₂NH
d) (CH₃)₃N
समाधान:
उत्तर: c) (CH₃)₂NH
व्याख्या: जलीय विलयन में द्वितीयक अमीन सबसे अधिक क्षारीय होते हैं क्योंकि:
- दो एल्किल समूह +I प्रभाव से नाइट्रोजन पर इलेक्ट्रॉन घनत्व बढ़ाते हैं
- हाइड्रेशन प्रभाव तृतीयक अमीन में अधिक स्टेरिक hindrance के कारण कम होता है
प्रश्न 2: गैब्रिएल संश्लेषण से कौन सा अमीन नहीं बन सकता?
a) मेथाइलएमीन
b) एनिलीन
c) डाइमेथाइलएमीन
d) एथाइलएमीन
समाधान:
उत्तर: c) डाइमेथाइलएमीन
व्याख्या: गैब्रिएल संश्लेषण केवल प्राथमिक अमीन बनाने के लिए उपयोग होता है। द्वितीयक अमीन नहीं बन सकते।
प्रश्न 3: हिंसबर्ग परीक्षा में कौन सा अमीन NaOH में घुलनशील उत्पाद देता है?
a) प्राथमिक अमीन
b) द्वितीयक अमीन
c) तृतीयक अमीन
d) सभी
समाधान:
उत्तर: a) प्राथमिक अमीन
व्याख्या: प्राथमिक अमीन से बना सल्फोनामाइड में N-H बंध होता है जो NaOH के साथ नमक बनाकर घुलता है।
संख्यात्मक प्रश्न (Numerical Problems)
प्रश्न 4: 0.1 M मेथाइलएमीन विलयन की pH ज्ञात करें। (Kb = 4.4 × 10⁻⁴)
समाधान:
CH₃NH₂ + H₂O ⇌ CH₃NH₃⁺ + OH⁻
Kb = [CH₃NH₃⁺][OH⁻]/[CH₃NH₂]
Kb = x²/(0.1-x) ≈ x²/0.1
4.4 × 10⁻⁴ = x²/0.1
x² = 4.4 × 10⁻⁵
x = [OH⁻] = 6.6 × 10⁻³ M
pOH = -log(6.6 × 10⁻³) = 2.18
pH = 14 - 2.18 = 11.82केस स्टडी आधारित प्रश्न (Case Study Based Questions)
प्रश्न 5: एक रसायनशास्त्री के पास तीन अज्ञात अमीन A, B, और C हैं। प्रयोगों से पता चला:
- A हिंसबर्ग परीक्षा में अवक्षेप देता है जो NaOH में घुलता है
- B कार्बाइलएमीन परीक्षा में सकारात्मक परिणाम देता है
- C NaNO₂ + HCl के साथ डायजोनियम नमक बनाता है
इन अमीनों की पहचान करें और अपना उत्तर सिद्ध करें।
समाधान:
- A: प्राथमिक एलिफैटिक अमीन (हिंसबर्ग परीक्षा सकारात्मक, NaOH में घुलनशील)
- B: प्राथमिक अमीन (कार्बाइलएमीन परीक्षा केवल 1° अमीन के लिए सकारात्मक)
- C: प्राथमिक एरोमैटिक अमीन (डायजोटाइजेशन केवल ArNH₂ के लिए संभव)
आरेख आधारित प्रश्न (Diagram Based Questions)
प्रश्न 6: निम्नलिखित अमीन की संरचना बनाएं और उनका IUPAC नाम लिखें:
a) N-एथाइल-N-मेथाइलप्रोपेन-2-एमीन
b) 4-ब्रोमोएनिलीन
समाधान:
a) (CH₃)₂CHCH₂N(CH₃)(C₂H₅) – तृतीयक अमीन
b) Br-C₆H₄-NH₂ (para position में Br) – प्राथमिक एरोमैटिक अमीन
10: परीक्षा रणनीति और उत्तर लेखन तकनीक (Exam Strategy and Answer Writing Techniques)
महत्वपूर्ण टॉपिक्स की प्राथमिकता (Priority Topics)
उच्च प्राथमिकता (High Priority):
- अमीन का वर्गीकरण और नामकरण – हर साल आता है
- तैयारी विधियां – गैब्रिएल संश्लेषण विशेष रूप से महत्वपूर्ण
- भौतिक गुण – क्वथनांक, घुलनशीलता, क्षारीयता
- पहचान परीक्षाएं – हिंसबर्ग, कार्बाइलएमीन, डायजोटाइजेशन
मध्यम प्राथमिकता (Medium Priority):
- एनिलीन के विशेष गुण
- अमीन की रासायनिक अभिक्रियाएं
- औद्योगिक महत्व
उत्तर लेखन की रणनीति (Answer Writing Strategy)
संरचित उत्तर तकनीक:
1. परिभाषा प्रश्न (1 अंक):
- स्पष्ट, संक्षिप्त परिभाषा
- उदाहरण दें (यदि स्थान हो)
- रासायनिक सूत्र लिखें
उदाहरण:
“अमीन वे कार्बनिक यौगिक हैं जो अमोनिया (NH₃) के हाइड्रोजन परमाणुओं को एल्किल या एरिल समूहों द्वारा प्रतिस्थापित करने से बनते हैं। उदाहरण: CH₃NH₂ (मेथाइलएमीन)”
2. अभिक्रिया प्रश्न (2-3 अंक):
- संतुलित रासायनिक समीकरण
- अभिक्रिया की परिस्थितियां
- उत्पाद का नाम
उदाहरण:
गैब्रिएल संश्लेषण:
C₆H₄(CO)₂NH + KOH → C₆H₄(CO)₂NK + H₂O
C₆H₄(CO)₂NK + RX → C₆H₄(CO)₂NR + KX
C₆H₄(CO)₂NR + NaOH + H₂O → RNH₂ + C₆H₄(COONa)₂3. तुलनात्मक प्रश्न (3-5 अंक):
- तालिका या बिंदुओं में व्यवस्थित करें
- स्पष्ट अंतर दिखाएं
- उदाहरण सहित व्याख्या
सामान्य गलतियां और बचने के तरीके (Common Mistakes and Prevention)
Common Error Alert:
रासायनिक सूत्र संबंधी गलतियां:
गलत: (CH₃)₃NH+ (तृतीयक अमीन में प्रोटोनेशन)
सही: (CH₃)₃NH+ (तृतीयक अमीन में भी प्रोटोनेशन हो सकता है)
नामकरण की गलतियां:
गलत: N-methyl-N-ethylamine (द्वितीयक अमीन के लिए)
सही: N-methylethanamine या N-ethylmethanamine
अभिक्रिया की परिस्थितियां:
गलत: डायजोटाइजेशन सामान्य तापमान पर
सही: डायजोटाइजेशन 0-5°C पर
निष्कर्ष और भविष्य की संभावनाएं (Conclusion and Future Prospects)
अमीन का अध्ययन केवल एक अकादमिक विषय नहीं है, बल्कि यह आधुनिक रसायन विज्ञान और जीवन विज्ञान की आधारशिला है। इस अध्याय में हमने देखा कि कैसे साधारण अमोनिया से शुरू होकर जटिल जैविक अणुओं तक, अमीन हर जगह मौजूद हैं।
मुख्य सीख (Key Takeaways):
संरचनात्मक समझ: अमीन की संरचना समझना महत्वपूर्ण है क्योंकि यह उनके सभी गुणों को नियंत्रित करती है। नाइट्रोजन का अकेला इलेक्ट्रॉन युग्म ही अमीन को विशेष बनाता है।
गुण-संरचना संबंध: हमने देखा कि कैसे हाइड्रोजन बंधन, अनुनाद, और स्टेरिक प्रभाव अमीन के भौतिक और रासायनिक गुणों को प्रभावित करते हैं।
तैयारी की कला: विभिन्न तैयारी विधियों का ज्ञान न केवल परीक्षा के लिए बल्कि भविष्य में रसायन विज्ञान के क्षेत्र में काम के लिए भी आवश्यक है।
पहचान की तकनीक: पहचान परीक्षाएं सिखाती हैं कि कैसे रासायनिक गुणों का उपयोग करके व्यावहारिक समस्याओं का समाधान किया जाता है।
भविष्य की दिशाएं (Future Directions):
Current Research में अमीन:
- नैनो मेडिसिन: अमीन-functionalized nanoparticles कैंसर के targeted therapy में उपयोग हो रहे हैं
- ग्रीन केमिस्ट्री: बायो-डिग्रेडेबल अमीन-based catalysts का विकास
- एनर्जी स्टोरेज: लिथियम-एयर बैटरी में अमीन-based electrolytes
करियर अवसर:
यदि आप अमीन में गहरी रुचि रखते हैं, तो निम्नलिखित क्षेत्रों में करियर बना सकते हैं:
- फार्मास्युटिकल रिसर्च: नई दवाओं का विकास
- एग्रोकेमिकल: पेस्टिसाइड और फर्टिलाइजर का विकास
- मटेरियल साइंस: स्मार्ट पॉलिमर का डिजाइन
- बायोटेक्नोलॉजी: प्रोटीन इंजीनियरिंग
जैसा कि आप इस अध्याय को पूरा करते हैं, याद रखें कि आप केवल परीक्षा की तैयारी नहीं कर रहे, बल्कि एक ऐसे विषय को सीख रहे हैं जो आपके आसपास की दुनिया को समझने में मदद करता है। अमीन की यह यात्रा आपको एक बेहतर छात्र, एक जिज्ञासु वैज्ञानिक, और एक सजग नागरिक बनने में मदद करेगी।
Solvefy का यह लेख आपको CBSE कक्षा 12 की परीक्षा में न केवल अच्छे अंक दिलाने के लिए तैयार किया गया है, बल्कि अमीन की गहरी समझ भी प्रदान करता है। नियमित अभ्यास, अवधारणा की स्पष्टता, और आत्मविश्वास के साथ आप निश्चित रूप से सफलता प्राप्त करेंगे।
Recommended –
- CBSE Board 2026: The Ultimate Preparation Guide – Study Plan, Time Table, Best Books & Topper Strategies
- CBSE कक्षा 12 रसायन विज्ञान अध्याय 7: अल्कोहल, फिनोल और ईथर – नोट्स, NCERT समाधान व महत्वपूर्ण प्रश्न (2025-26)
- कक्षा 12 रसायन विज्ञान अध्याय 8: एल्डिहाइड, कीटोन और कार्बोक्जिलिक अम्ल – नोट्स, NCERT समाधान व प्रश्न

